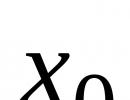Lipoproteíny (Lipoproteíny) - čo to je. Samostatnou úlohou je transport lipidov Hlavné skupiny sérových lipoproteínov
Hlavné lipidy nachádzajúce sa v krvnej plazme sú cholesterol, triglyceridy a fosfolipidy. Pre organizmus sú životne potrebné na vykonávanie mnohých funkcií, ale vzhľadom na ich vlastnosti, najmä ich nerozpustnú štruktúru, sú proteíny - apolipoproteíny - potrebné na ich prenos do buniek tkanív a orgánov. Väzbou na ne sa lipidy môžu voľne pohybovať spolu s prietokom krvi.
Lipoproteíny krvnej plazmy sú teda komplexom proteínov a lipidov, ktoré majú vo vode rozpustnú štruktúru, čo im umožňuje aktívne sa zapájať do metabolických procesov.
Všetky známe lipoproteíny obsahujú cholesterol, triglyceridy a fosfolipidy, ale ich pomery sa líšia v závislosti od frakcie lipidovej zlúčeniny. Lipoproteíny sa líšia aj v iných parametroch: veľkosť zlúčeniny, skupiny apoproteínu, rýchlosť flotácie, hustota komplexu.
Klasifikácia lipoproteínov
Dnes je známych veľa rôznych klasifikácií lipidových komplexov, ale najznámejšia a najobľúbenejšia je klasifikácia podľa poradia, v ktorom sa lipoproteíny pohybujú od štartovacej čiary v gravitačnom poli pri ultracentrifugácii.
Rozlišujú sa tieto frakcie lipoproteínov:
- (HM);
- lipoproteíny s nízkou hustotou (LDL);
- (VLDL);
- lipoproteíny so strednou hustotou (IDL);
- hustota (HDL).
Prítomnosť týchto zlúčenín v krvi je určená biochémiou alebo lipidovým profilom.
Každá skupina lipoproteínov má rôzne veľkosti častíc obsiahnutých v zlúčenine a obsah bielkovín v nich je tiež odlišný. Uvažujme v tabuľke o hlavných charakteristikách transportných foriem lipidov.
Tabuľka porovnávacích charakteristík lipoproteínov
| HM | LDL | VLDL | BOB | HDL | |
|---|---|---|---|---|---|
| Obsah bielkovín, % | 2 | 22 | 10 | 11 | 50 |
| Obsah cholesterolu, % | 2 | 8 | 7 | 8 | 4 |
| Veľkosť častíc, nm | 75-1200 | 18-26 | 30-80 | 25-35 | 8-11 |
| Miesto vzdelávania | Epitel tenkého čreva | Krv | Pečeňové bunky | Krv | Pečeňové bunky |
| Funkcie | Transport mastných kyselín a cholesterolu, ktoré pochádzajú z potravy, z čreva do pečeňových buniek a periférnych tkanív. | Transport lipidov z pečeňových buniek do periférnych tkanív. | Stredná forma konverzie VLDL na LDL. | Transport lipidov z periférnych tkanív do pečeňových buniek, odstránenie nadbytočného cholesterolu z iných lipoproteínov a buniek tela. |
Všetky menované frakcie lipoproteínov sú navzájom neoddeliteľne spojené, poskytujú bunkám tela primeranú výživu a sú základom biochémie mnohých procesov. Ak sa pod vplyvom rôznych faktorov pozoruje porucha metabolizmu lipoproteínov, naruší sa prirodzená rovnováha lipidov v krvi a v tele sa začnú rozvíjať patologické procesy, z ktorých hlavným je aterosklerotické poškodenie ciev. Pozrime sa na tieto krvné lipoproteíny podrobnejšie.
Chylomikróny
K tvorbe týchto krvných lipoproteínov dochádza v epitelových bunkách čreva po strávení potravy a absorpcii tukov z tenkého čreva. Potom sa dostanú do medzibunkového priestoru a ďalej sa vstrebávajú do lymfatických kapilár klkov. Sú to najväčšie lipoproteínové zlúčeniny v priemere.

Chylomikróny transportujú cholesterol, triglyceridy a exogénne mastné kyseliny v krvi. 85 % cholesterolu pozostáva z triglyceridov, preto sú klasifikované ako lipoproteíny bohaté na triglyceridy. Tieto lipidové zlúčeniny sú nevyhnutné na transport triglyceridov v prvých hodinách po požití. Predpokladá sa, že normálne 12 hodín po poslednom jedle úplne zmiznú z krvnej plazmy.
Počas metabolizmu lipidov sa tieto komplexy vyskytujú v krvi s lipoproteínmi s vysokou hustotou a vymieňajú si rôzne podtypy proteínov - apoproteíny. Pri ich rozklade sa uvoľňujú estery cholesterolu a bielkoviny, z ktorých časť je viazaná lipoproteínmi s vysokou hustotou a zvyšok sa dostáva do pečeňových buniek, tam sa premieňa a vylučuje z tela.
LDL
Táto frakcia lipoproteínov sa považuje za najviac aterogénnu, pretože obsahuje v priemere 45 % cholesterolu a je jeho hlavnou transportnou formou, pričom zároveň uľahčuje transport karotenoidov, triglyceridov, vitamínu E a niektorých ďalších zložiek. Okrem toho sa v týchto zlúčeninách koncentruje asi 60 až 70 % všetkého sérového cholesterolu.

Pri procese lipolýzy tieto zlúčeniny vznikajú z VLDL, pričom vo výslednom komplexe klesá obsah triglyceridov a naopak stúpa cholesterol. Tieto štruktúry sú teda konečným štádiom metabolizmu lipidov produkovaných pečeňovými bunkami.
Predpokladá sa, že je to koncentrácia týchto lipoproteínov v krvi, ktorá úplnejšie odráža pravdepodobnosť aterosklerotických lézií cievnych stien, dokonca aj hladina cholesterolu je v tomto ohľade menej dôležitá.
V dôsledku porúch metabolizmu lipoproteínov s nízkou hustotou, najmä v smere zvyšovania ich hladiny v krvi, začínajú u človeka vznikať vážne ochorenia, najmä ak sa včas nezačne normalizácia. Dôvody takéhoto porušenia môžu byť:
- zlá výživa;
- ochorenia pečene;
- dedičné poruchy metabolizmu lipidov;
- fajčenie a nadmerná konzumácia alkoholu;
- endokrinné ochorenia;
- sedavý spôsob života.
Aby ste tento ukazovateľ neustále monitorovali, musíte každý rok robiť biochémiu krvi a ak sa zistí najmenšia odchýlka od normy, prijmite vhodné opatrenia.
VLDL
Táto frakcia lipoproteínov má podobné zloženie a štruktúru ako chylomikróny, ale je menšia. Obsahujú menej triglyceridov, ale viac apolipoproteínov, fosfolipidov a cholesterolu. V tomto prípade sú VLDL spolu s chylomikrónmi klasifikované ako lipoproteíny bohaté na triglyceridy.

Miesto syntézy týchto komplexov sa nazýva pečeňové bunky a ich hlavnou úlohou je transport triglyceridov vytvorených v tom istom orgáne. Tieto komplexy tiež transportujú cholesterol, cholesterylestery a fosfolipidy do buniek tela.
Rýchlosť tvorby týchto lipoproteínových frakcií sa mení v závislosti od určitých podmienok: zvyšuje sa so zvýšeným prísunom voľných mastných kyselín a veľkého množstva sacharidov do pečene.
VLDL sú prekurzory lipoproteínov s nízkou hustotou, pretože v dôsledku hydrolýzy pôsobením enzýmu lipoproteínová lipáza sa prvé rozpadnú a vytvorí sa intermediárna forma lipidov - LDLP, ktoré sa následne premieňajú na LDL. rovnakej hydrolýzy.
VLDL sa nazývajú vysoko aterogénne zlúčeniny, pretože patria medzi zdroje „zlého“ cholesterolu v tele. Ak sú tieto komplexy zvýšené v krvi, vytvára to predpoklady pre rozvoj aterosklerózy a jej následkov. Za hlavný dôvod zvýšenia ich hladiny sa považuje dedičná predispozícia a nadmerný príjem živočíšnych tukov z potravy. Iné príčiny tejto patológie môžu byť:
- ochorenia pečene a žlčníka;
- endokrinné poruchy;
- obezita;
- alkoholizmus;
- ochorenie obličiek, najmä v chronickej forme.
BOB
Tieto štruktúrne zlúčeniny sa tvoria v krvnej plazme pri premene VLDL na LDL a často sa nazývajú zvyškové VLDL. Pod vplyvom enzýmu lipoproteínová lipáza sa lipoproteíny s veľmi nízkou hustotou transformujú na inú formu - LDLP, z ktorých polovica je úplne eliminovaná z tela v procese zložitých biochemických reakcií a druhá časť v dôsledku hydrolýzy účasť pečeňovej lipázy sa mení na LDL.
Zloženie týchto častíc sa podobá kríženiu medzi kompozíciami lipoproteínov s nízkou a veľmi nízkou hustotou. Zistilo sa, že u zdravých ľudí v krvi odobratej nalačno tieto komplexy buď úplne chýbajú, alebo ich koncentrácia je desaťkrát nižšia ako hladina LDL.
Hlavným dôvodom zvýšenia koncentrácie týchto zlúčenín v krvnej plazme je vraj dedičná predispozícia a strava bohatá na živočíšne tuky. Tento faktor prispieva k rozvoju kardiovaskulárnych ochorení.
HDL
Tieto zlúčeniny sa nazývajú antiaterogénne, pretože nevedú k zvýšeniu hladiny „zlého“ cholesterolu v krvi, ale naopak, keď sú v dostatočnej koncentrácii, prispievajú k jeho viazaniu a odstráneniu z tela. Tvoria sa v pečeňových bunkách a sú z polovice zložené z bielkovín, teda majú najvyššiu možnú hustotu. Zároveň je ich obsah cholesterolu minimálny. Majú najmenšiu veľkosť a majú tvar disku, preto sa HDL v úzkych kruhoch označuje ako „disky“.

K syntéze týchto častíc dochádza v pečeňových bunkách, po uvoľnení z nich sa viažu na fosfolipidy a začínajú interagovať s inými frakciami lipoproteínov a telesnými bunkami, zachytávajú cholesterol a získavajú plnohodnotnú formu lipidovej zlúčeniny. Takto HDL dodáva nadbytočný cholesterol späť do pečeňových buniek, kde podlieha rozkladu a vylučovaniu cez gastrointestinálny trakt.
Inými slovami, dochádza k neustálej výmene cholesterolu medzi LDL a HDL, pričom tok cholesterolu smeruje k HDL. „Dobré“ lipoproteíny prijímajú cholesterolové bunky od „zlých“, potom ich transportujú do pečene na následné spracovanie na žlčové kyseliny. Opísaný proces sa nazýva jediný prirodzený spôsob odstránenia cholesterolu z tela, preto sa pre zdravie srdca a ciev odporúča vždy udržiavať optimálnu hladinu HDL v krvnej plazme.
Lipoproteínové modifikácie
Pre stanovenie rizika vzniku kardiovaskulárnych ochorení sú dôležité nielen samotné lipoproteíny, ale aj ich modifikované formy. Lipoproteíny môžu byť modifikované z normálnych frakcií, čím vznikajú patologické zlúčeniny. Hlavnými dôvodmi tohto procesu sú: uvoľňovanie voľných radikálov bunkami; zvýšená koncentrácia glukózy v krvi; uvoľňovanie produktov metabolizmu lipidov do krvi.
Nasledujú najvýznamnejšie modifikované lipoproteíny:
- Lipoproteín (a) je špeciálny typ lipoproteínu s nízkou hustotou, ktorý sa líši len v niektorých štruktúrnych znakoch. Polypeptidový proteínový reťazec je teda dodatočne pripojený k bunke lipoproteínu (a). To vedie k tomu, že lipoproteíny (a) sa selektívne začínajú hromadiť na stenách krvných ciev a v nich sa vyvíja zápalový proces.
- Oxidovaný LDL. V dôsledku vstupu veľkého množstva voľných radikálov do krvi dochádza k oxidácii lipidov LDL membrán a vnášaniu produktov peroxidácie lipidov do nich. Tento proces iniciuje vznik penových buniek, ktoré sa stávajú stavebným materiálom aterosklerotických plátov.
- Glykovaný LDL. Keď sa glukóza naviaže na lipoproteínové proteíny s nízkou hustotou, zmení sa ich štruktúra. Sú modifikované a vo svojej novej štruktúre sú schopné zotrvať v krvnom obehu, pričom podliehajú ďalšej oxidácii a ukladajú sa na stenách krvných ciev.
- Malé, husté LDL. Patria do najvýznamnejšej skupiny modifikovaných aterogénnych zlúčenín. Obsahujú dostatočné množstvo cholesterolu a fosfolipidov, pričom ich štruktúra je podobná arteriálnym bunkám. V dôsledku komplexnej biochémie sa z mLDL uvoľňujú všetky fosfolipidy a cholesterol, ktoré sa následne ukladajú na vaskulárnom endoteli.
- Upravené HDL. Pri syntéze HDL v pečeňových bunkách sa uvoľňujú niektoré zlúčeniny s defektmi, ktorých vlastnosti prenášajú modifikovaný HDL z kategórie antiaterogénnych do aterogénnych.
Prítomnosť týchto komplexov v krvnej plazme vedie k narušeniu metabolizmu tukov v tele, ktoré je plné aterosklerotických zmien v krvných cievach. Modifikované lipoproteíny môžu byť rozpoznané pomocou podrobného lipidového profilu. Takáto štúdia sa musí vykonať, ak existuje podozrenie na závažné ochorenia v tele, ako aj s ich dedičnými formami.
Hladiny v krvi
Najdôležitejším spôsobom, ako určiť riziko vzniku kardiovaskulárnych ochorení, je biochémia krvi. Normy boli vypočítané pre každú lipoproteínovú frakciu. Ak ich výsledok prekročí alebo zníži, naznačuje to potrebu ďalšieho výskumu na potvrdenie existujúcich chorôb. Normy lipoproteínov v krvi sú uvedené v nasledujúcej tabuľke:
Pre ženy majú tieto ukazovatele svoje vlastné normy, ktoré sú spojené s niektorými charakteristikami ženského tela. Môže to zahŕňať nižšiu telesnú hmotnosť, špeciálne hormonálne pozadie (najmä obsah inhibínu B a hormónu stimulujúceho folikuly v krvi) a zodpovedajúce vlastnosti metabolických procesov v tele. Preto pre ženy bude takáto tabuľka vyzerať takto:
Ak sa získané výsledky mierne líšia od normy, potom korekcia výživy pomôže predchádzať ateroskleróze a normalizuje metabolizmus lipidov. V opačnom prípade môže byť potrebná vážna lieková terapia.
Poznamenalo sa, že pomerne často u žien počas tehotenstva, prvých 6 týždňov po pôrode, perimenopauze a menopauze, sa tieto ukazovatele môžu výrazne líšiť od normálnych hodnôt. Takéto výsledky možno považovať za normálne (berúc do úvahy individuálne charakteristiky), ak pacient nemá v anamnéze ochorenia pečene, štítnej žľazy, hypofýzy, obličiek a niektorých ďalších orgánov.
Zvýšenie aterogénnych frakcií lipoproteínov (LDL, VLDL), ako aj zníženie lipoproteínov s vysokou hustotou u mužov a žien môže naznačovať prítomnosť nasledujúcich ochorení:
- ateroskleróza;
- angina pectoris;
- infarkt myokardu;
- akýkoľvek typ hyperlipidémie;
- dedičná hyperlipidémia a hypercholesterolémia;
- narušenie produkcie hormónov štítnej žľazy, a to v smere nárastu aj poklesu;
- choroby hypofýzy;
- ochorenia obličiek (nefrotický syndróm, chronické zlyhanie obličiek);
- ochorenia pečene (chronické zlyhanie pečene, porfýria, niektoré typy hepatitídy);
- ochorenia pankreasu, najmä pankreatitída a malignita;
- intoxikácia alkoholom;
- obezita;
- metabolické patológie (napríklad dna).
Na potvrdenie väčšiny uvedených patológií samotná biochémia krvi nestačí, budú potrebné ďalšie diagnostické štúdie. Stojí za to pochopiť, že niektoré stavy (napríklad tehotenstvo) alebo užívanie liekov môžu ovplyvniť výsledok biochémie krvi. Preto by sa takéto funkcie mali prediskutovať so svojím lekárom, pretože by mali byť uvedené v odporúčaní na krvný test. Aj keď žena užíva antikoncepčné tabletky, musí ich buď na dva týždne prestať užívať, alebo túto skutočnosť uviesť vo formulári pri absolvovaní lipidového profilu.
Aterogénne a antiaterogénne frakcie lipoproteínov
V posledných rokoch došlo k širokému rozšíreniu aterosklerózy, ktorá je spojená predovšetkým s rozvojom ochorenia hyperlipoproteinémia a hypercholesterolémia v organizme, ktoré tento stav zvyčajne sprevádzajú. Zistilo sa, že rozvoj aterosklerózy priamo súvisí so zvýšením aterogénnych lipoproteínov - LDL a VLDL v krvi (to sú najviac aterogénne lipidové zlúčeniny). Súčasne sa v krvnej plazme znižuje koncentrácia lipoproteínov s vysokou hustotou, jediných antiaterogénnych frakcií lipoproteínov.

Medzi aterogénne lipoproteíny patrí aj DILI, ale ich koncentrácia v krvi nie je v procese hodnotenia rizika aterosklerózy taká dôležitá, keďže tieto frakcie sú intermediárne lipidy.
Ako už bolo popísané vyššie, LDL frakcia transportuje endogénny cholesterol do periférnych tkanív; HDL robí opačnú prácu - uvoľňuje cholesterolové bunky z lipoproteínov s nízkou hustotou a telesných buniek, potom ich dodáva do pečene na následné spracovanie na žlč a odstránenie z telo prirodzene. Z tohto dôvodu je optimálna hladina antiaterogénnych lipoproteínových frakcií taká dôležitá pre metabolizmus lipidov a prevenciu tvorby aterosklerotických plátov na stenách krvných ciev.
Pokiaľ ide o chylomikróny, stojí za zmienku, že tieto komplexy samotné nemajú aterogénne vlastnosti. Ich zvyškové zložky však môžu byť aterogénne.
Na určenie rizika rozvoja kardiovaskulárnych ochorení sa používa koeficient aterogenity, ktorý sa vypočíta podľa tohto vzorca:
KA = (celkový cholesterol - HDL)/HDL.

Normálne u mužov a žien by mal byť tento index v rozmedzí 2-3 jednotiek. Ak je to viac ako tri, naznačuje to vysoké riziko aterosklerózy. Pacienti s výsledkom väčším ako 5 by mali pochopiť, že v ich cievach už prebiehajú aterosklerotické procesy. Ak je tento indikátor menší ako dva, potom v tele nie sú žiadne zvláštne poruchy metabolizmu lipidov, ale tento výsledok môže byť vyvolaný niektorými inými ochoreniami (napríklad obličky, pečeň).
Na posúdenie zdravotného stavu lekári odporúčajú absolvovať biochémiu krvi ročne a jej rozšírenú formu, kde sa stanovujú všetky lipoproteíny krvnej plazmy, raz za 5 rokov. To umožní včas odhaliť poruchy metabolizmu lipidov a prijať vhodné opatrenia na zabránenie vzniku závažných ochorení kardiovaskulárneho systému.
LIPIDY sú vo vode nerozpustné zlúčeniny, preto ich transport v krvi vyžaduje špeciálne nosiče, ktoré sú rozpustné vo vode. Takýmito transportnými formami sú LIPOPROTEÍNY. Patria medzi voľné LIPIDY. Syntetizovaný tuk v črevnej stene, prípadne tuk syntetizovaný v iných tkanivách a orgánoch, môže byť transportovaný krvou až po zaradení do zloženia LIPOPROTEÍNOV, kde bielkoviny zohrávajú úlohu stabilizátora.
Micely LIPOPROTEIN majú podľa svojej štruktúry vonkajšiu vrstvu a jadro. Vonkajšia vrstva je vytvorená z PROTEÍNOV, FOSFOLIPIDOV a CHOLESTEROLU, ktoré majú hydrofilné polárne skupiny a vykazujú afinitu k vode. Jadro tvoria TRIGLYCERIDY, CHOLESTEROL ESTERY, IVF, vitamíny A, D, E, K.T.o. nerozpustné tuky sa po syntéze v črevnej stene, ako aj syntéze v iných tkanivách medzi bunkami, ktoré ich syntetizujú a využívajú, ľahko transportujú do celého tela.
Existujú 4 triedy krvných LIPOPROTEÍNOV, ktoré sa navzájom líšia chemickým stavom, veľkosťou miciel a transportovanými tukmi. Pretože majú rôznu rýchlosť sedimentácie v roztoku kuchynskej soli, delia sa na:
1. CHYLOMIKRÓNY. Tvoria sa v črevnej stene a majú najväčšiu veľkosť častíc.
2. VLDL. Syntetizovaný v črevnej stene a pečeni.
3. LDL. Tvoria sa v endoteli kapilár z VLDL.
4. HDL. Tvorí sa v črevnej stene a pečeni.
To. transportné krvné lipidy sú syntetizované dvoma typmi buniek – ENTEROCYTMI a HEPATOCYTMI. Zistilo sa, že krvné lipidy sa pri elektroforéze bielkovín pohybujú v zóne alfa a beta GLOBULÍNOV, takže ich elektroforetická pohyblivosť je stále
označené ako:
Pre-beta-LP = VLDL,
Beta-LP=LDL,
Alfa-LP = HDL.
ryža. Chemické zloženie krvných lipoproteínov
CHYLOMIKRÓNY (CM), ako najväčšie častice počas elektroforézy, zostávajú na začiatku.
Ich maximálna koncentrácia sa dosiahne 4 - 6 hodín po jedle. Rozdelili sa
vplyvom enzýmu - LIPOPROTEID LIPÁZY, ktorý sa tvorí v pečeni, pľúcach a tukovom tkanive
po príjme potravy sú KM transportované prevažne TRIacylGLYCERIDMI (až 83 %).
VLDL a LDL transportujú hlavne cholesterol a jeho estery do buniek orgánov a tkanív. Tieto frakcie sú klasifikované ako ATEROGÉNNE. HDL sa zvykne označovať ako ANTI-ATEROGÉNNY LP, ktorý transportuje CHOLESTEROL (nadbytočný cholesterol uvoľnený v dôsledku rozpadu bunkových membrán) do pečene k následnej oxidácii za účasti cytochrómu P450 za tvorby žlčových kyselín, ktoré sa vylučujú z telo vo forme KOPROSTEROLOV. Krvné LIPOPROTEÍNY sa po endocytóze rozkladajú v LYZOZÓMOCH a MIKROZÓMOCH: pôsobením LIPOPROTEID LIPÁZY v bunkách pečene, obličiek, nadobličiek, tukového tkaniva čreva, endotelu kapilár. Produkty hydrolýzy liečiva sa podieľajú na bunkovom metabolizme.
Lipoproteíny pozostávajú z lipidov a bielkovín. Sú potrebné na transport cholesterolu do buniek, ktoré ho využívajú. Nerovnováha v tomto systéme vedie k rozvoju závažných ochorení.
Termín lipoproteíny označuje komplexné organické komplexy vytvorené z lipidov a špeciálnych proteínov podieľajúcich sa na transporte hydrofóbnych molekúl. Cholesterol, fosfolipidy, triglyceridy – všetky tieto látky patria medzi lipidy. To znamená, že sa nerozpúšťajú vo vode, ale môžu sa s ňou za určitých podmienok iba miešať a vytvárať emulzie.
Lipoproteíny a lipoproteíny sú synonymá, ale pojem lipoproteíny sa častejšie spomína na transportné formy voľného cholesterolu, ako aj jeho esterov. Keďže cholesterol sa podieľa na syntéze životne dôležitých hormónov a stavbe bunkových membrán, jeho dodávanie do periférnych tkanív v tele zohráva významnú úlohu.
Typy lipoproteínov sa líšia hustotou a nábojom na povrchu. Tieto vlastnosti určujú ich pohyblivosť v elektromagnetickom poli a separáciu na frakcie pri centrifugácii.Klinicky najvýznamnejšie sú tieto typy lipoproteínov:
- chylomikróny;
- pre-lipoproteíny;
- na lipoproteíny alebo beta;
- a lipoproteíny alebo alfa.
Každý z týchto typov sa tvorí v tkanivách a vykonáva špecifické funkcie. Majú podobné zloženie, líšia sa však pomerom lipidov a bielkovín. Vo všeobecnosti je portrét jednotlivého lipoproteínu určený kvalitou proteínových molekúl, vďaka čomu je komplex rozpoznateľný pre rôzne bunky v tele.
V laboratórnych štúdiách boli lipoproteíny po prvýkrát rozdelené na frakcie centrifugáciou. Ukázalo sa, že pľúca sú v hornej časti skúmavky a tie s väčšou hustotou v spodnej časti. Odtiaľ pochádzajú ďalšie názvy, ktoré označujú hustotu jednotlivých zlomkov.
Lipoproteíny s veľmi nízkou hustotou sa nazývajú ľahšie ako voda. Z nich sa tvoria lipoproteíny patriace do frakcie s nízkou hustotou, ktoré si zaslúžia pomenovanie „zlé“. A „dobré“ alfa lipoproteíny sa nazývajú vysokohustotné, sú ťažšie ako voda.
Pri určovaní pravdepodobnosti vzniku srdcových a cievnych ochorení sa posudzuje celková hladina cholesterolu, frakcie jednotlivých lipoproteínov a ich pomer. Zníženie počtu „zlých“ znamená zníženie pravdepodobnosti infarktu alebo mŕtvice.
Chylomikróny
Najväčšími a najľahšími zástupcami triedy lipoproteínov sú chylomikróny, ktoré sa tvoria v črevnej stene a slúžia ako obal pre tuky dodávané s potravou. Veľká veľkosť neumožňuje tejto frakcii preniknúť priamo do krvi. Z hrúbky črevnej steny vstupujú do celkového krvného obehu, najprv prechádzajú sieťou lymfatických kapilár.
Zloženie chylomikrónov obsahuje iba 2% bielkovín a 5% cholesterolu s jeho estermi. Sú ľahšie ako voda, pretože sú nabité triacylglyceridmi, inými slovami, tukmi. Po jedle začnú chylomikróny prenikať do krvnej plazmy, čo jej dodáva opalescentný vzhľad
mlieko. Niekoľko hodín vykonávajú svoju prácu a dodávajú lipidové molekuly bunkám, ktoré to potrebujú.
Pri vyšetrovaní pacientov biochemický krvný test hodnotí množstvo triacylglyceridov prenášaných chylomikrónmi. Menej ako 12 hodín po poslednom jedle budú hodnoty zvýšené a nepresné. Analýza sa vykonáva na prázdny žalúdok. U zdravých ľudí po 12–14 hodinách hladovania nie sú v krvnej plazme žiadne chylomikróny.
Norma triacylglyceridov u mužov je 0,45–1,81 mmol/l, u žien je norma 0,40–0,53 mmol/l. Hodnoty sa u mužov a žien líšia vplyvom pohlavných hormónov.
Lipoproteíny s veľmi nízkou hustotou
Táto trieda lipoproteínov zatiaľ nedostala jednoznačné hodnotenie od lekárskej komunity. Ich úloha pri rozvoji aterosklerózy nebola spoľahlivo stanovená a optimálna hladina pre mužov a ženy nebola stanovená. Ich množstvo v tele sa zvyšuje u ľudí, ktorí zneužívajú alkohol.
Tvoria sa v pečeni a slúžia ako transportná forma pre endogénny cholesterol. Vplyvom enzýmov v krvnej plazme sa v dôsledku prenosu bielkovín z lipoproteínu a. tvoria na lipoproteíny.
Beta lipoproteíny
Lipoproteíny s nízkou hustotou si vyslúžili označenie „zlé“ pre svoju vysokú aterogenitu. Ich zloženie zahŕňa 55% cholesterolu, ale iba 22% bielkovín. Asi 70 % všetkého cholesterolu v tele sa prenesie na lipoproteíny, čo je hlavná transportná forma na dodávanie cholesterolu do tkanív. Bez tejto funkcie, ktorú vykonávajú lipoproteíny, je životne dôležitá syntéza bunkových membrán a steroidných hormónov nemožná.
Beta lipoproteíny v krvi sa tvoria z lipoproteínov s veľmi nízkou hustotou pôsobením enzýmu lipoproteín lipázy. Jediný typ proteínu zahrnutý v ich zložení je charakteristický znak, ktorý umožňuje bunkám rozpoznať tento komplex a zachytiť ho z krvi. Obnova bunkových membrán, syntéza vitamínu D a steroidných hormónov priamo závisí od tejto funkcie.
Bunky zachytávajú lipoproteíny z krvi interakciou s proteínom, ktorý tvorí komplex s lipidmi. Počet receptorov v tele nie je konštantný a závisí od pôsobenia hormónov.
To vysvetľuje, prečo ateroskleróza často komplikuje priebeh niektorých ochorení endokrinného systému, preto ich treba redukovať.
Počet receptorov sa zvyšuje pod vplyvom inzulínu a hormónov štítnej žľazy. U pacientov s cukrovkou alebo hypotyreózou sú beta lipoproteíny často zvýšené, rovnako ako riziko vzniku srdcových príhod. Pacienti by mali prísne dodržiavať diétu, znížiť množstvo sacharidov a užívať lieky.
Ak je hladina steroidných hormónov zvýšená, zvyšuje sa tým aj riziko aterosklerózy. Hormóny kôry nadobličiek môžu znižovať tvorbu receptorov. U žien vo fertilnom veku sú vďaka estrogénom zriedkavo zvýšené „zlé“ lipoproteíny.
Norma pre lipoproteíny s nízkou hustotou pre mužov a ženy nie je vyššia ako 3,36 mmol / l.
Alfa lipoproteíny
Lipoproteín a plní dve hlavné funkcie: transportuje cholesterol z tkanív do pečene a dodáva molekuly proteínov iným lipoproteínom. Obsahujú 50 % bielkovín a asi 20 % cholesterolu. Pečeňové bunky a črevná stena syntetizujú nezrelé alfa-lipoproteíny, pod vplyvom enzýmov krvnej plazmy sa mení počet molekúl proteínov a lipidov, ktoré tvoria úplný komplex.
 Alfa lipoproteíny sú ťažšie ako voda a najrýchlejšie sa pohybujú v elektrickom poli. Norma pre lipoproteín a pre mužov a ženy je 0,92–1,95 mmol/l.
Alfa lipoproteíny sú ťažšie ako voda a najrýchlejšie sa pohybujú v elektrickom poli. Norma pre lipoproteín a pre mužov a ženy je 0,92–1,95 mmol/l.
Dyslipoproteinémia
Komplexný dynamický proces výmeny lipidov a proteínov medzi rôznymi triedami lipoproteínov prebieha nepretržite. Narušenie týchto procesov sa prejavuje nerovnováhou, keď sú niektoré látky zvýšené, znížené alebo chýbajú. Dyslipoproteinémia môže byť dedičná alebo sekundárna, sprevádzajúca poruchy endokrinného systému a metabolizmu.
Familiárna hyperlipoproteinémia
Genetické abnormality ktoréhokoľvek z proteínov, ktoré tvoria lipoproteínové komplexy, vedú k rozvoju závažných patológií. Defektné gény neovplyvňujú pohlavné chromozómy, choroby postihujú rovnako mužov aj ženy.
Hladiny triacylglyceridov a cholesterolu v krvi sú zvýšené. Pamäť ľudí sa zhoršuje skoro, v dôsledku zúženia priesvitu krvných ciev dochádza k silným bolestiam brucha, k narušeniu funkcií pankreasu.
Príznaky koronárnej nedostatočnosti sa začínajú objavovať v dospievaní. Pacienti sú vystavení riziku vzniku včasného, pred 30. rokom života, infarktu myokardu. Riziko možno znížiť prísnym dodržiavaním diéty s obmedzeným množstvom tuku a užívaním statínov.
Akantocytóza
Defekt v géne kódujúcom tvorbu jedného proteínu „zlých“ lipoproteínov vedie k rozvoju akantocytózy. Ochorenie sa dedí bez ohľadu na pohlavie a vyskytuje sa u mužov a žien.
Pri znížení lipoproteínov je narušený transport cholesterolu, potrebného na stavbu membrán, buniek nervového systému a krvi. V dôsledku poškodenia myelínových obalov neurónov dochádza k neurologickým poruchám a zhoršeniu zraku. Životnosť červených krviniek sa znižuje a vzniká anémia.
Telo neabsorbuje tuky z potravy, hromadia sa v pečeni a črevách a vzniká nedostatok vitamínov rozpustných v tukoch. Pacientom sa odporúča jesť stravu s obmedzením živočíšnych tukov a užívať veľké dávky vitamínu E.
Modifikované lipoproteíny
K modifikáciám lipoproteínov dochádza, keď sú vystavené určitým enzýmom, protilátkam, produktom peroxidácie alebo glukóze. Tento vplyv mení vlastnosti molekúl bielkovín a tým aj metabolické dráhy. Najviac aterogénne sú modifikované lipoproteíny. Usádzajú sa na stenách tepien, poškodzujú ich a vytvárajú aterosklerotické pláty.
Keď je hladina glukózy v krvi zvýšená, jej pripojenie k lipoproteínovým komplexom narúša ich normálny metabolizmus. To vysvetľuje skorší vývoj aterosklerózy u ľudí s cukrovkou.
Hlavnými lipidmi v ľudskej krvnej plazme sú triglyceridy, fosfolipidy a cholesterylestery. Tieto zlúčeniny sú estery mastných kyselín s dlhým reťazcom a ako lipidová zložka sú spoločne zahrnuté v zložení lipoproteínov. Tuk
kyseliny sú v plazme prítomné aj vo voľnej (neesterifikovanej) forme.
Zásobníkom mastných kyselín je tukové tkanivo a využívajú sa v pečeni a svaloch, kde sú transportované vo forme voľných mastných kyselín (FFA). Mastné kyseliny, najmä kyselina palmitová, olejová a linolová, sa ukladajú v tukovom tkanive vo forme triglyceridov. Rýchlosť mobilizácie triglyceridov je určená prácou lipázy citlivej na hormóny, ktorej aktivita sa zvyšuje pod vplyvom určitých hormónov, ako je norepinefrín a glukokortikoidy. Lipolýza vedie k uvoľňovaniu mastných kyselín a glycerolu do plazmy a zvyšuje sa v podmienkach akútneho stresu, dlhodobého hladovania a nedostatku inzulínu.
Triglyceridy (alebo triacylglyceridy) sú estery mastných kyselín a glycerolu. K syntéze triglyceridov v pečeni a tukovom tkanive dochádza glycerofosfátovou cestou, zatiaľ čo v tenkom čreve sa triglyceridy tvoria hlavne v dôsledku priamej esterifikácie monoglyceridov absorbovaných z potravy. Triglyceridy resyntetizované v bunkách tenkého čreva sa uvoľňujú do črevných lymfatických ciev vo forme chylomikrónov a potom vstupujú do krvného obehu cez hrudný lymfatický kanál. Normálne sa absorbuje viac ako 90 % triglyceridov. To znamená, že denne sa do krvi dostane 70-150 g exogénnych triglyceridov. V tenkom čreve dochádza k tvorbe takzvaných endogénnych triglyceridov, ktoré sú syntetizované z endogénnych mastných kyselín, no ich hlavným zdrojom je pečeň, odkiaľ sa vylučujú vo forme lipoproteínov s veľmi nízkou hustotou (VLDL). Rozsah zvyškov mastných kyselín nachádzajúcich sa v triglyceridoch a VLDL závisí vo veľkej miere od zloženia triglyceridových mastných kyselín dodávaných v strave.
Dva hlavné fosfolipidy, ktoré sú prítomné v plazme, sú fosfatidylcholín (lecitín) a sfingomyelín. K syntéze fosfolipidov dochádza takmer vo všetkých tkanivách, ale hlavným zdrojom plazmatických fosfolipidov je pečeň. Fosfolipidy sú neoddeliteľnou súčasťou všetkých bunkových membrán. Medzi plazmou a červenými krvinkami prebieha neustála výmena lecitínu a sfingomyelínu. Oba tieto fosfolipidy sú prítomné v plazme ako zložky lipoproteínov, kde hrajú kľúčovú úlohu pri udržiavaní rozpustného stavu nepolárnych lipidov, ako sú triglyceridy a cholesterylestery.
Cholesterol je sterol obsahujúci steroidné jadro so štyrmi kruhmi a hydroxylovú skupinu. Táto zlúčenina sa v tele nachádza ako voľný sterol aj ako ester s jednou z mastných kyselín s dlhým reťazcom. Voľný cholesterol -
súčasť všetkých bunkových membrán a hlavná forma, v ktorej je cholesterol prítomný vo väčšine tkanív. Výnimkou je kôra nadobličiek, plazma a ateromatózne pláty, kde prevládajú estery cholesterolu. Väčšina tkanív má schopnosť syntetizovať cholesterol, ale normálne sa takmer všetok cholesterol syntetizuje v pečeni a distálnom tenkom čreve.
Prvým krokom syntézy cholesterolu je premena acetátu na kyselinu mevalónovú. Enzým, ktorý určuje rýchlosť tohto procesu, sa nazýva 3-hydroxy-3-metylglutaryl-coenim A reduktáza (HMG-CoA reduktáza). Aktivita tohto enzýmu je regulovaná na princípe spätnej väzby konečným produktom reakcie, cholesterolom. Hlavnými metabolitmi cholesterolu sú žlčové kyseliny,
- syntetizované výlučne v pečeni. Kľúčovým enzýmom je v tomto prípade cholesterol-7-alfa-hydroxyláza.
Viac ako dve tretiny cholesterolu v plazme sú esterifikované predovšetkým kyselinou linolovou a olejovou. Tieto estery vznikajú najmä v plazme pôsobením enzýmu lecitín-cholesterol acyl-transferázy (LCAT). Pomerne malý podiel na tomto procese má aj enzým tenkého čreva a pečene – ACAT. Povaha esterov cholesterolu závisí vo veľkej miere od mastných kyselín
zloženie plazmatického lecitínu alebo, inými slovami, od typu tuku v potravinách. Na rozdiel od svojich esterov sa voľný plazmatický cholesterol ľahko vymieňa za cholesterol bunkovej membrány.
Bežne sa hladina celkového cholesterolu (TC) v krvnej plazme pohybuje od 4 do 6,5 mmol/l, no na rozdiel od hladiny triglyceridov sa po konzumácii mastných jedál prudko nezvyšuje.
Všetky lipidy, s výnimkou voľných mastných kyselín, vstupujú do plazmy vo forme makromolekulárnych komplexov nazývaných lipoproteíny. Tieto komplexy obsahujú špecifické proteínové zložky, apolipoproteíny (apoproteíny alebo jednoducho apo), ktoré interagujú s fosfolipidmi a voľným cholesterolom a tvoria polárny vonkajší obal, ktorý chráni nepolárne triglyceridy a cholesterylestery umiestnené vo vnútri.
Pomocou ultracentrifugácie krvnej plazmy odobratej darcovi po jedle je možné rozlíšiť šesť tried lipoproteínov. Všetky sú to sférické častice rôznej veľkosti a pozostávajúce zo zmesi proteínov, fosfolipidov, triglyceridov, voľného a esterifikovaného cholesterolu, ktorých relatívne množstvá sa líšia medzi rôznymi triedami lipoproteínov. Väčšina cholesterolu sa teda nachádza v lipoproteínoch s nízkou hustotou (LDL) a podstatne menšia časť sa nachádza vo VLDL a lipoproteínoch s vysokou hustotou (HDL). Na rozdiel od cholesterolu sú endogénne triglyceridy transportované primárne ako súčasť VLDL. Chylomikróny slúžia na transport triglyceridov v prvých hodinách po jedle a normálne úplne vymiznú z plazmy po 12 hodinách nalačno. Meranie celkového cholesterolu a triglyceridov v plazme alebo sére teda poskytuje súčet príspevkov každej triedy lipoproteínov. Zmeny hladín lipidov v sére zvyčajne odrážajú zmeny buď v koncentráciách lipoproteínov, alebo v pomere hladín rôznych tried lipoproteínov. Normálne je koncentrácia zvyškových častíc alebo lipoproteínov strednej hustoty (IDL) v plazme relatívne nízka a ich prínos sa spravidla zanedbáva, ale môže byť rozhodujúci pri meraní cholesterolu a triglyceridov v krvi pacientov s niektorými formami hyperlipidémie.
Pred popisom metabolizmu rôznych tried lipoproteínov je potrebné urobiť krátky prehľad fyzikálnych vlastností týchto častíc samotných a apolipoproteínov, ktoré ich obsahujú. Plazmové lipoproteíny sa líšia rýchlosťou flotácie, hydratovanou hustotou, veľkosťou a elektroforetickou pohyblivosťou. V súčasnosti je najbežnejšia klasifikácia lipoproteínov založená na rozdieloch v ich hustote, čo sa používa na separáciu týchto častíc ultracentrifugáciou. Okrem toho sú lipoproteíny
Výrazne sa líšia aj obsahom apolipoproteínov, čiže apoproteínov.
Apoproteíny plnia tri hlavné funkcie: 1) interagujú s fosfolipidmi, pomáhajú solubilizovať estery cholesterolu a triglyceridy; 2) regulovať reakcie lipoproteínových lipidov s enzýmami, ako je LCAT, lipoproteínová lipáza a pečeňová lipáza; 3) viažu sa na receptory na povrchu buniek, čím určujú miesta zachytenia a rýchlosť degradácie iných zložiek, najmä cholesterolu. Väzba apoproteínov na lipidy nastáva primárne prostredníctvom hydrofóbnych interakcií medzi reťazcami mastných kyselín fosfolipidov a nepolárnymi oblasťami apoproteínov. Iónové interakcie medzi polárnymi skupinami fosfolipidových hláv a pármi opačne nabitých aminokyselín apoproteínov zohrávajú sekundárnu stabilizačnú úlohu.
Apolipoproteíny rodiny A, apo A-I a apo A-II, sú hlavnými proteínovými zložkami HDL. Existujú dôkazy, že keď sú oba apoproteíny A blízko seba, ako je to v prípade HDL, apo A-II zosilňuje lipidové väzbové vlastnosti apo A-I. Ďalšou funkciou apo A-I je aktivácia enzýmu LCAT
Apoproteín B alebo apo B je charakterizovaný heterogenitou a variáciami v molekulovej hmotnosti; apo BSO0 sa nachádza hlavne v chylomikrónoch, VLDL a LDL, a apo B48 sa nachádza iba v chylomikrónoch. V tomto prípade apo BSO0 slúži ako ligand pre LDL receptor, ale apo B48 nie.
Apoproteín C zahŕňa aspoň tri jednotlivé apoproteíny, ktoré sú hlavnými zložkami VLDL a vedľajšou zložkou HDL. Predpokladá sa, že apo C-II aktivuje enzým lipoproteín lipázu.
Apoproteín E, zložka VLDL, LPPP a HDL, vstupuje do plazmy hlavne ako súčasť novosyntetizovaného HDL. Apo E vykonáva niekoľko funkcií, vrátane receptorom sprostredkovaného prenosu cholesterolu medzi tkanivami a plazmou.
Ďalšie apoproteíny zahŕňajú apo D, minoritnú zložku HDL; apo A-IV, ktorý sa nachádza v črevných chylomikrónoch; ako aj apo(a), jednu z proteínových zložiek špeciálneho lipoproteínu (a) alebo LP(a). V súčasnosti literatúra obsahuje podrobné prehľady moderných údajov o štruktúre a funkciách apolipoproteínov.
Lipoproteíny jednotlivých tried zohrávajú v aterogenéze rôznu úlohu, a preto je potrebné uviesť ich stručnú charakteristiku.
Chylomikróny sú najväčšie lipoproteínové častice, majú priemer od 100 do 1000 nm a obsahujú prevažne triglyceridy
dy, ako aj malé množstvá fosfolipidov, voľného cholesterolu, jeho esterov a bielkovín. Hlavnou funkciou chylomikrónov je transport potravinových triglyceridov z čreva, kde sú absorbované, do krvného obehu.
VLDL (pre-β-lipoproteíny) majú podobnú štruktúru a zloženie ako chylomikróny, ale majú menšiu veľkosť, od 25 do 100 nm, a obsahujú menej triglyceridov, ale viac cholesterolu, fosfolipidov a bielkovín. VLDL sa od chylomikrónov líši miestom syntézy a zdrojom transportovaných triglyceridov. VLDL sa teda tvorí hlavne v pečeni a slúži na transport endogénnych triglyceridov.
Rýchlosť tvorby VLDL sa zvyšuje so zvýšeným prietokom voľných mastných kyselín vstupujúcich do pečene, ako aj v situáciách, keď sa zvyšuje rýchlosť syntézy endogénnych mastných kyselín v pečeni, ku ktorej dochádza, keď do tela vstupuje veľké množstvo uhľohydrátov. .
Častice VLDL sa líšia veľkosťou. V dôsledku lipolýzy vznikajú malé VLDL – nazývajú sa remnantné VLDL alebo lipoproteíny so strednou hustotou (IDL), ktoré sú medziproduktom v procese premeny VLDL na LDL. Pri hypertriglyceridémii dochádza nielen k zvýšeniu počtu, ale aj veľkosti VLDL, čo môže byť pravdepodobne príčinou ďalšieho charakteristického znaku tohto ochorenia – poklesu hladiny LDL.
LDL f-lipoproteíny) sú hlavnou triedou plazmatických lipoproteínov, ktoré transportujú cholesterol. Tieto častice sa líšia od svojich prekurzorov VLDL tým, že majú výrazne nižší obsah triglyceridov a prítomnosť iba jedného apo B100 z rôznych apoproteínov nachádzajúcich sa vo VLDL. Katabolizmus LDL závisí od faktorov prostredia, napríklad od typu konzumovaného tuku, ako aj od genetických faktorov, ako sú mutácie v génoch kódujúcich receptor LDL a apo B.
HDL (a-lipoproteíny) sa delia na podtriedy HDL2 a HDL3 na základe rozsahu ich hustoty. Viac ako 90 % HDL proteínu predstavuje proteín apo A. HDL sa syntetizuje v pečeni a tenkom čreve. Akumulácia cholesterylesterov v retikuloendoteliálnom systéme pacientov, ktorým chýba HDL (Tangierova choroba), naznačuje, že HDL normálne hrá vedúcu úlohu pri odstraňovaní tkanivového cholesterolu.
LP (a) je väčší ako LDL, ale má v porovnaní s nimi vyššiu hustotu a má elektroforetickú pohyblivosť charakteristickú pre VLDL. Lipoproteín (a) sa z hľadiska lipidového zloženia nelíši od LDL, má však viac bielkovín, vrátane vlastného apo (a) – podľa
lymorfný proteín, ktorý má vysoký stupeň homológie s plazminogénom a obsahuje väčšie množstvo sacharidov. Existujú dôkazy, že lipoproteín(a) sa tvorí výlučne v pečeni, bez ohľadu na metabolizmus VLDL.
Metabolizmus lipoproteínov je komplexný dynamický a do značnej miery neprebádaný proces, ktorý zahŕňa ako rôzne pohyby lipidov a apoproteínov medzi jednotlivými triedami lipoproteínov, tak množstvo reakcií katalyzovaných enzýmami. Tieto interakcie vedú okrem iného k receptorom sprostredkovanému vstupu cholesterolu do bunky alebo k jeho odstráneniu z bunky.
Tu je vhodné pripomenúť, že funkcia apoproteínov nie je obmedzená len na to, že tvoria s lipidmi rozpustné, a teda krvou transportovateľné komplexy. Zistilo sa, že niektoré apoproteíny vykonávajú koenzýmovú úlohu, aktivujúc určité reakcie metabolizmu lipidov. Najmä apo A-I aktivuje reakciu uskutočňovanú LCAT.Pri tejto reakcii, ako je známe, dochádza k esterifikácii voľného cholesterolu v krvnej plazme. Existujú dôkazy, že LCAT reakcia je tiež katalyzovaná apo C-I.
Apo C-II sa ukázalo ako nevyhnutná zložka pre reakcie katalyzované lipoproteínovými lipázami. Keďže pôsobením lipoproteínovej lipázy dochádza k rozkladu triglyceridov chylomikrónov a VLDL, táto reakcia nadobúda osobitný význam ako počiatočný krok v katabolizme týchto lipoproteínov.
V roku 1985 dostali americkí vedci J. Goldstein a M. Brown Nobelovu cenu za objav LDL receptora a zistenie príčiny familiárnej hypercholesterolémie. Zistili, že hlavnou úlohou LDL receptora je poskytnúť všetkým bunkám tela dostupný zdroj cholesterolu, ktorý je nevyhnutný pre syntézu bunkových membrán a niektoré orgány ho využívajú aj ako substrát na tvorbu určitých produktov. ich metabolizmu, napríklad žlčové kyseliny, pohlavné hormóny, kortikosteroidy. Preto bunky pečene, pohlavných žliaz a nadobličiek obsahujú veľké množstvo LDL receptorov. Pečeň je vďaka svojej veľkosti hlavným miestom receptorom sprostredkovaného katabolizmu LDL. LDL receptory tiež viažu zvyšok VLDL (alebo LDLP) a jednu z podtried HDL, ktorá má apo-E proteín.
Koordinovaná regulácia expresie LDL receptora a aktivity HMG-CoA reduktázy zabezpečuje fungovanie homeostatického mechanizmu zásobovania cholesterolom bunky, ako sú hepatocyty, ktoré ho denne spracovávajú veľké množstvá. Farmakologické látky, ktoré kompetitívne inhibujú HMG-CoA-re-
duktázy, blokujú endogénnu syntézu cholesterolu a tým stimulujú expresiu LDL receptora, čo vedie k zníženiu hladiny LDL cholesterolu v krvnej plazme.
HDL receptor bol identifikovaný v kultivovaných fibroblastoch a bunkách hladkého svalstva. Expresia tohto receptora sa zvyšuje, keď sú bunky zaťažené cholesterolom. Okrem toho boli opísané dva ďalšie lipoproteínové receptory, hoci ich príspevok k metabolizmu lipoproteínov in vivo nebol stanovený.
V zjednodušenej forme môže byť intracelulárny a tkanivový metabolizmus lipoproteínov rôznych tried znázornený nasledovne. Chylomikróny dodávajú potravinové lipidy do krvnej plazmy cez lymfu. Pod vplyvom extrahepatálnej lipoproteínovej lipázy, aktivovanej a-po C-II, sa chylomikróny v plazme premieňajú na zvyšky, ktoré sú zachytené hepatocytovými receptormi, ktoré rozpoznávajú povrchový apo-E. Endogénne triglyceridy sú prenášané VLDL z pečene do plazmy, kde podobne ako chylomikróny podliehajú čiastočnej degradácii na zvyškový VLDL alebo RLD. Na druhej strane je DILI buď zachytený LDL receptormi, ktoré rozpoznávajú apo E alebo apo BSO, alebo je konvertovaný na LDL obsahujúci apo BSO, ale už nemá apo E. V tomto procese môže byť zahrnutá pečeňová lipáza. Katabolizmus LDL sa vyskytuje dvoma hlavnými spôsobmi, z ktorých jeden je spojený s receptormi LDL a druhý s pečeňovou triglyceridovou lipázou. HDL má komplexný pôvod: jeho lipidová zložka zahŕňa buď voľný cholesterol a fosfolipidy uvoľnené počas lipolýzy chylomikrónov a VLDL, alebo voľný cholesterol pochádzajúci z periférnych buniek, pričom hlavný apoproteín HDL, apo A-I, sa syntetizuje v pečeni aj v tenké črevo. Novosyntetizované častice HDL v plazme sú reprezentované podtriedou HDL3, ale v konečnom dôsledku sa vplyvom LCAT aktivovaného apo A-I premenia na HDL2. Bohužiaľ, zatiaľ nemáme presné údaje o postupnosti zostavovania lipoproteínových častíc, nehovoriac o mechanizmoch tohto procesu.
Tabuľka 1.1
Rozsah kolísania obsahu celkového cholesterolu (TC), triglyceridov (TG), LDL-C a HDL-C v krvnej plazme (v mmol/l) je v norme.
|
Vek, roky |
HCO |
TG |
LDL-C |
HDL-C |
|
0-19 |
3.2-5.2 |
0.4-1.5 |
1.7-3.4 |
1.0-1.9 |
|
20-29 |
3.2-5.9 |
0.5-2.1 |
1.8-4.3 |
0.8-1.7 |
|
30-39 |
3.7-6.8 |
0.6-3.2 |
2.1-4.9 |
0.8-1.7 |
|
40-49 |
4.0-7.0 |
0.6-3.5 |
2.3-5.0 |
0.8-1.7 |
|
50-59 |
4.1-7.2 |
0.7-3.3 |
2.3-5.2 |
0.8-1.7 |
Zloženie, štruktúra a klasifikácia krvných lipoproteínov. Úloha rôznych tried lipoproteínov v patogenéze hyperlipoproteinémie. Doplnil: Khapez A.E. Skupina: 218 b Západokazašská štátna lekárska univerzita pomenovaná po Maratovi Ospanovovi Nezávislá študentská práca
Relevantnosť plánu 1. Zloženie, štruktúra, klasifikácia a fyziologická úloha krvných lipoproteínov. 2. Tvorba chylomikrónov a transport tukov. 3. Úloha rôznych tried lipoproteínov v tele a patogenéza hyperlipoproteinémie. 4. Biochémia aterosklerózy. 5. Poruchy metabolizmu cholesterolu. Záver Zoznam referencií

Význam Vysoké hladiny lipoproteínov v krvnej plazme sú rizikovým faktorom koronárnej choroby srdca, aterosklerózy, trombózy a mŕtvice. Vysoká hladina lipoproteínu, podobne ako vysoká hladina LDL, určuje riziko vzniku skorej aterosklerózy. Štúdium základných vlastností lipoproteínov umožní presnejšiu diagnostiku týchto ochorení, pomôže aj pri ich prevencii a liečbe.

Zloženie a štruktúra lipoproteínov krvnej plazmy Lipoproteíny sú komplexy lipidov s proteínmi. Všetky typy lipoproteínov majú podobnú štruktúru – hydrofóbne jadro a hydrofilnú vrstvu na povrchu. Hydrofilnú vrstvu tvoria proteíny nazývané apoproteíny a amfifilné molekuly lipidov – fosfolipidy a cholesterol. Hydrofilné skupiny týchto molekúl smerujú k vodnej fáze a hydrofóbne časti smerujú k hydrofóbnemu jadru lipoproteínu, ktorý obsahuje transportované lipidy.

Klasifikácia lipoproteínov krvnej plazmy Lipoproteíny krvnej plazmy sa klasifikujú podľa ich hustoty: chylomikróny (CM) lipoproteíny s veľmi nízkou hustotou (VLDL) lipoproteíny so strednou hustotou (IDL) lipoproteíny s nízkou hustotou (LDL) lipoproteíny s vysokou hustotou (HDL)



Fyziologická úloha lipoproteínov krvnej plazmy Apoproteíny v zložení lipoproteínov plnia nielen štrukturálnu funkciu, ale zabezpečujú aj aktívnu účasť lipidových komplexov na transporte lipidov v krvnom obehu z miest ich syntézy do buniek periférnych tkanív, ako napr. ako aj spätný transport cholesterolu do pečene na ďalšie metabolické premeny. Apoproteíny pôsobia ako ligandy pri interakcii liečiv so špecifickými receptormi na bunkových membránach, čím regulujú homeostázu cholesterolu v bunkách a v tele ako celku. Nemenej významná je apoproteínová regulácia aktivity radu základných enzýmov metabolizmu lipidov: lecitín-cholesterol acyltransferáza, lipoproteínová lipáza, pečeňová triglyceridová lipáza.

Tvorba chylomikrónov Hlavným apoproteínom v zložení KM je proteín apoB-48. Tento proteín je kódovaný v rovnakom géne ako proteín VLDL – B-100, ktorý sa syntetizuje v pečeni. Proteín apoB-48 sa syntetizuje v hrubom ER a je tam glykozylovaný. Potom v Golgiho aparáte dochádza k tvorbe CM, nazývaných „nezrelé“. Mechanizmom exocytózy sa vylučujú do chyle, ktorý sa tvorí v lymfatickom systéme črevných klkov, a cez hlavný hrudný lymfatický kanál sa dostávajú do krvi. V lymfe a krvi sa apoproteíny E (apoE) a C-P (apoS-P) prenášajú z HDL do CM; XM sa menia na „zrelé“.

Transport tukov chylomikrónmi V krvi sú triacylglyceroly, ktoré sú súčasťou zrelých KM, hydrolyzované enzýmom lipoproteínová lipáza alebo LP lipáza. LP lipáza hydrolyzuje molekuly tuku na glycerol a 3 molekuly mastných kyselín. V dôsledku pôsobenia LP lipázy na CM tuky vznikajú mastné kyseliny a glycerol. Väčšina mastných kyselín preniká do tkanív. V tukovom tkanive sa v období vstrebávania ukladajú mastné kyseliny vo forme triacylglycerolov, v srdcovom svale a pracujúcich kostrových svaloch sa využívajú ako zdroj energie. Ďalší produkt hydrolýzy tukov, glycerol, je rozpustný v krvi a transportuje sa do pečene, kde sa môže počas doby vstrebávania využiť na syntézu tukov.


Úloha rôznych tried lipoproteínov v tele a patogenéza hyperlipoproteinémie Hyperhypoproteinémia (HLP) je zvýšenie určitej triedy alebo tried lipoproteínov v krvi. Podľa verzie WHO sa rozlišujú nasledujúce typy SLP. Typ I - hyperchylomikronémia. Hlavné zmeny sú nasledovné: vysoký obsah CM, normálny alebo mierne zvýšený obsah VLDL; prudko zvýšené hladiny triglyceridov v krvnom sére. Klinicky sa tento stav prejavuje xantomatózou. Typ II sa delí na dva podtypy: typ IIa - hyper-β-hypoproteinémia s charakteristickým vysokým obsahom LDL v krvi a typ IIb - hyper-β-lipoproteinémia s vysokým obsahom dvoch tried lipoproteínov súčasne (LDL, VLDL) . Pri type II je vysoký a v niektorých prípadoch veľmi vysoký obsah cholesterolu v krvnej plazme. Hladina triglyceridov v krvi môže byť buď normálna (typ aIIa) alebo zvýšená (typ IIb). Klinicky sa prejavuje aterosklerotickými poruchami, často sa rozvinie ischemická choroba srdca (ICHS).

Úloha rôznych tried lipoproteínov v organizme a patogenéza hyperlipoproteinémie Typ III – tis-β-hypoproteinémia. V krvnom sére sa objavujú lipoproteíny s nezvyčajne vysokým obsahom cholesterolu a vysokou elektroforetickou pohyblivosťou („plávajúce“ β-lipoproteíny). Hromadia sa v krvi v dôsledku porušenia konverzie VLDL na LDL. Tento typ HLP sa často kombinuje s rôznymi prejavmi aterosklerózy, vrátane ochorenia koronárnych artérií a poškodenia krvných ciev nôh. Typ IV – hyperpre-β-hypoproteinémia. Charakterizované zvýšením hladín VLDL, normálnymi hladinami LDL a absenciou CM; zvýšené hladiny triglyceridov s normálnou alebo mierne zvýšenou hladinou cholesterolu. Klinicky sa tento typ kombinuje s cukrovkou, obezitou a ochorením koronárnych artérií. Typ V – hyperpre-β-hypoproteinémia a hyperchylomikroémia. Pozoruje sa zvýšenie hladín VLDL a prítomnosť CM. Klinicky sa prejavuje xantomatózou, niekedy kombinovanou s latentným diabetom. Koronárna choroba srdca sa pri tomto type HLP nepozoruje.

Biochémia aterosklerózy Jednou z hlavných príčin vzniku aterosklerózy je nerovnováha medzi príjmom cholesterolu z potravy, jeho syntézou a vylučovaním z tela. 1. štádium Proces začína poškodením vaskulárneho endotelu v dôsledku zmenenej štruktúry LDL. Škody spôsobujú voľné radikály vznikajúce počas metabolizmu alebo prichádzajúce zvonku. Pri LDL sa mení nielen štruktúra samotných lipidov, ale narúša sa aj štruktúra apoproteínov. Oxidovaný LDL je vychytávaný makrofágmi cez vychytávacie receptory. Tento proces nie je regulovaný množstvom absorbovaného cholesterolu, ako v prípade jeho vstupu do buniek cez špecifické receptory, takže makrofágy sú preťažené cholesterolom a menia sa na „penové bunky“, ktoré prenikajú do subendotelového priestoru. To vedie k tvorbe tukových pruhov v stene krvných ciev.

Biochémia aterosklerózy Stupeň 2 V tomto štádiu si vaskulárny endotel môže zachovať svoju štruktúru. Keď sa počet „penových buniek“ zvyšuje, dochádza k poškodeniu vaskulárneho endotelu. Normálne endotelové bunky vylučujú prostaglandín I 2 (prostacyklín I 2), ktorý inhibuje agregáciu krvných doštičiek. Pri poškodení endotelových buniek sa aktivujú krvné doštičky. Po prvé, vylučujú tromboxán A2, ktorý stimuluje agregáciu krvných doštičiek, čo môže viesť k tvorbe krvnej zrazeniny v oblasti aterosklerotického plátu; po druhé, krvné doštičky začnú produkovať peptid - rastový faktor odvodený od krvných doštičiek, ktorý stimuluje proliferáciu SMC. SMC migrujú z mediálnej vrstvy do vnútornej vrstvy arteriálnej steny a tým prispievajú k rastu plaku.

Biochémia aterosklerózy Stupeň 3 Ďalej plaketa rastie s fibróznym tkanivom (kolagén, elastín); bunky pod vláknitou membránou nekrotizujú a cholesterol sa ukladá v medzibunkovom priestore. V tomto štádiu sa v strede plaku tvoria dokonca kryštály cholesterolu. 4. fáza Plak je nasýtený vápenatými soľami a stáva sa veľmi hustým. V oblasti plaku sa často tvoria krvné zrazeniny, ktoré blokujú lúmen cievy, čo vedie k akútnym poruchám krvného obehu v príslušnej oblasti tkaniva a rozvoju srdcového infarktu. Najčastejšie sa aterosklerotické plaky vyvíjajú v tepnách myokardu, takže najčastejším ochorením, ktoré sa vyvíja v dôsledku aterosklerózy, je infarkt myokardu.

Poruchy metabolizmu cholesterolu Hypercholesterolémia je nadbytok normálnej koncentrácie cholesterolu v krvi. Hypercholesterolémia sa často vyvíja v dôsledku nadmerného príjmu cholesterolu z potravy, ako aj sacharidov a tukov. Hyperkalorická výživa je jedným zo spoločných faktorov rozvoja hypercholesterolémie, pretože na syntézu cholesterolu sú potrebné iba acetyl-CoA, ATP a NADPH. Všetky tieto substráty vznikajú pri oxidácii glukózy a mastných kyselín, preto nadmerný príjem týchto zložiek potravy prispieva k rozvoju hypercholesterolémie. Bežne príjem cholesterolu z potravy znižuje syntézu vlastného cholesterolu v pečeni, ale s vekom sa účinnosť regulácie u mnohých ľudí znižuje.

Poruchy metabolizmu cholesterolu Akýkoľvek defekt LDL receptora alebo proteínu apoB-100, ktorý s ním interaguje, vedie k rozvoju najčastejšieho dedičného ochorenia – familiárnej hypercholesterolémie. Toto autozomálne dominantné ochorenie je spôsobené mutáciami v géne LDL receptora. Heterozygoti, ktorí majú jeden normálny gén a druhý defektný, sa vyskytujú s frekvenciou 1:500 ľudí. Homozygoti sú zriedkavé - 1: človek. Koncentrácie cholesterolu a LDL v krvi takýchto pacientov už v ranom detstve sú zvýšené 5-6 krát. LDL je vychytávaný makrofágmi prostredníctvom fagocytózy. Makrofágy, nabité nadbytočným cholesterolom a inými ligandami obsiahnutými v LDL, sa ukladajú v koži a dokonca aj v šľachách a vytvárajú takzvané xantómy. Cholesterol sa tiež ukladá v stenách tepien a vytvára aterosklerotické plaky. Takéto deti bez núdzových liečebných opatrení zomierajú vo veku 5-6 rokov.


Zoznam použitej literatúry: 1. Komarov F.I., Korovkin B.F. a Menshikov V.V. Biochemický výskum na klinike, s. 407, L., Metzler D. Biochemistry, trans. z angličtiny, zväzok 2, M., Nikolaev A.Ya. Biologická chémia, M., Biochémia: Učebnica. pre univerzity, Ed. E.S. Severina., 2003